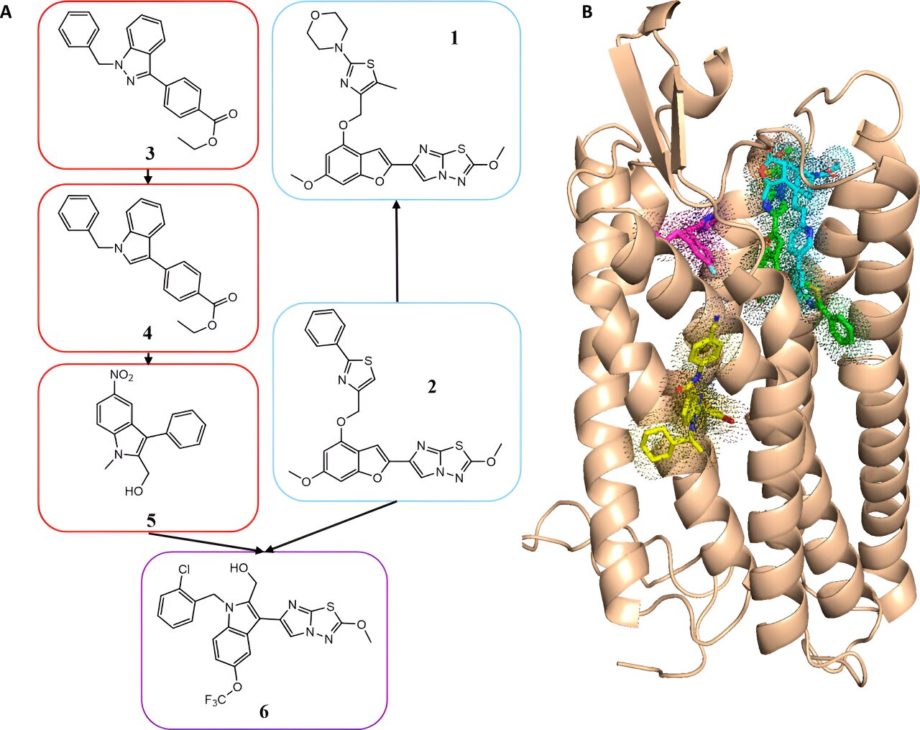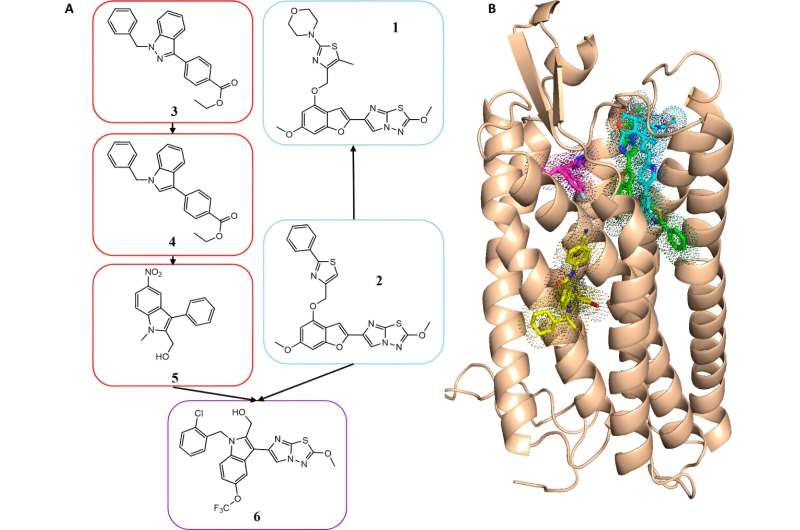
(A) Красные прямоугольники соответствуют оптимизации серий индолов с 3 по 4 и 5; светло-синий обозначает серию имидазотиадиазолов от BMS, начиная с BMS-3 (2) из HTS и BMS-986120 (1) в клинических исследованиях; фиолетовый обозначает серию химеризации ряда индола и имидазотиадиазола (6). (B) Прогнозируемый режим связывания BMS-3 (зеленый). Сравнение с экспериментально определенными режимами связывания: ворапаксар (PAR1, идентификатор PDB: 3vw7, голубой), AZ3451 (PAR2, идентификатор PDB: 5NDZ, желтый) и AZ8838 (PAR2, идентификатор PDB: 5NDD, пурпурный). Кредит: ACS Фармакология и трансляционная наука (2024). DOI: 10.1021/acptsci.3c00378.
Команда исследователей Вандербильта создала новую серию потенциальных лекарств против труднодоступного рецептора, участвующего в образовании тромбов. Исследование, возглавляемое лабораториями Йенса Мейлера, профессора-исследователя химии, Крейга Линдсли, исполнительного директора Уорреновского центра по поиску лекарств в области нейробиологии и профессора фармакологии, а также Хайди Хамм, профессора сердечно-сосудистых исследований Эйлин М. Ланге и Энни Мэри Лайл. и профессор фармакологии, была опубликована в ACS Фармакология и трансляционная наука в марте 2024 года.
Сгустки крови, затрудняющие кровоток (тромбоз), могут поразить любого человека и могут образовываться в венах, например, при тромбоэмболии легочной артерии, или в артериях, например, при сердечных приступах или инсультах. Хотя тромбоз не обязательно является смертельным, до начала пандемии только в США ежегодно регистрировалось от 100 000 до 300 000 смертей, связанных с тромбами, но с тех пор это число, вероятно, увеличилось. Согласно исследованию, проведенному в Великобритании в 2022 году, инфекция COVID-19 увеличивает риск возникновения у человека проблем, связанных со тромбами, сразу после заражения и в течение 49 недель после него.
Риск образования тромбов усугубляется определенными факторами риска, но его можно снизить с помощью таких препаратов, как антиагреганты, но они вызывают нежелательные побочные эффекты. Новые подходы к нацеливанию на тромбоциты, которые играют ключевую роль в образовании тромбов, включают активируемый протеазой рецептор 4; недавние данные лабораторий Вандербильта и других предполагают, что PAR4 также может быть жизнеспособной мишенью для лечения воспалительных заболеваний, таких как повреждение почек и болезнь Альцгеймера.
Однако, несмотря на очевидную привлекательность, PAR4 трудно нацелить. Рецептор клеточной поверхности PAR4 активируется, когда протеаза, называемая тромбином, расщепляет его хвост, в результате чего обнажается «новый» хвост (называемый привязанным лигандом), который взаимодействует с другими частями PAR4. Поскольку лиганд рецептора прикреплен к самому рецептору, оказалось сложно создать ингибитор PAR4, который мог бы превзойти привязанный лиганд и ингибировать PAR4.
«Основная техническая инновация возникла в результате применения скрининга сверхбольших библиотек для компьютерного проектирования лекарств. Этот подход позволил нам протестировать миллиарды молекул, подобных лекарству, на биологическую активность», — сказал Шеннон Смит, бывший аспирант лаборатория Мейлера и первый автор статьи.
Авторы использовали компьютерное моделирование, чтобы «пристыковать» 129 миллионов соединений к компьютерной модели PAR4. Новые антагонисты, идентифицированные в ходе скрининга, были затем улучшены с помощью медицинской химии в лаборатории Линдсли и протестированы на биологическое ингибирование рецептора. Хотя использование этого типа скрининга не является новым, такой скрининг никогда не проводился с белком без известной структуры — только с белками с известной кристаллической структурой.
«Поскольку в то время не было экспериментальной структуры PAR4, мы использовали модель PAR4 и смогли успешно разработать ряд соединений с биологической активностью», — сказал Смит. «Это открывает возможности для структурного, компьютерного дизайна лекарств для многочисленных целей без экспериментальных структур».
Лиганды PAR4, полученные в результате этого скрининга, представляют собой новую серию с фармакологией, отличной от более ранних семейств лигандов PAR4. Авторы будут использовать новую серию для дальнейшего изучения структуры и функции PAR4, а также того, как сами лиганды взаимодействуют с рецептором и ингибируют его. В конечном итоге они надеются, что их работа покажет другим исследователям, что PAR4 и другие подобные ему рецепторы не так сложны для воздействия, как они могли подумать поначалу.
«Способность блокировать активность PAR4 может обеспечить терапевтический подход к ряду хронических заболеваний, включая болезни сердца и инсульт, а также воспалительные состояния, такие как болезнь Альцгеймера», — сказал Хэмм. «Этот прорыв чрезвычайно интересен».
Больше информации:
Шеннон Т. Смит и др., Открытие антагонистов-лигандов, активируемых протеазой рецептора 4 (PAR4), с использованием сверхбольшого виртуального скрининга, ACS Фармакология и трансляционная наука (2024). DOI: 10.1021/acptsci.3c00378.
Предоставлено Медицинским факультетом фундаментальных наук Университета Вандербильта.
Цитирование: Новые кандидаты в лекарства, действующие на тромбы, разработанные с помощью компьютерного проектирования лекарств (11 июня 2024 г.), получены 12 июня 2024 г. с https://medicalxpress.com/news/2024-06-drug-candidates-blood-clots-aided.html.
Этот документ защищен авторским правом. За исключением любых добросовестных сделок в целях частного изучения или исследования, никакая часть не может быть воспроизведена без письменного разрешения. Содержимое предоставлено исключительно в информационных целях.