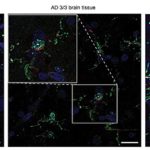
Крошечная стеклянная трубка (вверху слева) представляет собой электродную запись возбуждающего нейрона человека с болезнью Альцгеймера, созданную с использованием современных методов стволовых клеток (темно-синий, на кончике трубки). Фото: Исследование Скриппса.
По данным Центров США по контролю и профилактике заболеваний, по меньшей мере 5,8 миллиона американцев в настоящее время живут с болезнью Альцгеймера, которая является наиболее распространенной формой деменции. Лекарства от болезни Альцгеймера не существует, отчасти потому, что у ученых еще нет полного понимания того, что вызывает это заболевание. Но новое исследование Scripps Research проливает свет на молекулярные факторы, которые могут способствовать прогрессированию болезни Альцгеймера.
В исследовании, опубликованном в Передовая наукаИсследователи использовали новую технику для изучения одиночных живых клеток мозга, пораженных болезнью Альцгеймера. Измеряя электрическую активность отдельных нейронов и уровень белка внутри этих нейронов, ученые обнаружили новые молекулы, связанные с болезнью Альцгеймера. Есть надежда, что на эти молекулы можно будет воздействовать лекарствами для лечения или замедления прогрессирования нейродегенеративных заболеваний в будущем.
Тесное сотрудничество между профессорами Scripps Research, включая клинического невролога Стюарта Липтона, доктора медицинских наук, эксперта по белкам Джона Йейтса, III, доктора философии, и биоинформатика Николаса Шорка, доктора философии (который также является заместителем директора и выдающийся профессор количественной медицины в Научно-исследовательском институте трансляционной геномики (TGen) позволил ученым совершить этот биотехнологический подвиг.
«Меня поразило, что мы можем взять одну клетку, измерить ее электрическую активность порядка одной миллионной или одной миллионной ампера, а затем посмотреть на тысячи белков внутри этой же клетки, чтобы найти возможность найти белки, которые управляют аномальной электрической активностью, связанной с болезнью Альцгеймера», — говорит старший автор Липтон, который также является профессором Фонда Step Family и содиректором Центра новых лекарств нейродегенерации в Scripps Research. «Но прелесть этого метода в том, что он позволяет нам выявить новые мишени для лечения болезни Альцгеймера и связанных с ней деменций».
Предыдущие исследования Липтона и других показали, что определенные нейроны в мозгу людей с болезнью Альцгеймера становятся сверхактивными, посылая электрические сигналы сильнее и чаще, чем обычно. Имеющиеся данные свидетельствуют о том, что эта чрезмерная активность (также известная как гипервозбудимость) способствует снижению когнитивных функций, связанному с болезнью Альцгеймера.
В новой работе Липтон и его коллеги разработали систему, с помощью которой ученые могут проводить точные измерения отдельных клеток мозга, а затем сравнивать клетки, пораженные болезнью Альцгеймера, со здоровыми клетками. Группа Липтона, которая ранее разработала методы точного измерения электрической активности нейронов, объединилась с Йейтсом, чтобы использовать масс-спектрометрию для определения уровней более 2250 белков в каждой нервной клетке. Масс-спектрометрия позволяет идентифицировать и количественно определять белки в клетках, но этот анализ традиционно проводился на больших коллекциях клеток. Последние достижения позволяют проводить измерения на уровне отдельных клеток.
В новой системе, известной как одноклеточный (sc)Patch-Clamp/Proteomics, крошечная стеклянная трубка, наполненная раствором соли, используется в качестве электрода для измерения электрической активности клетки, а затем извлекается клетка для исследования белка с помощью масс-спектрометрии.
«Этот подход позволяет нам связать нарушения электрических функций с молекулярными событиями в нейронах, что является интересным применением протеомики», — говорит Йейтс.
Ученые проанализировали электрические закономерности и уровни белка около 150 нейронов, а затем использовали вычислительные инструменты, примененные Шорком, чтобы найти связь между гипервозбудимостью и аномальными уровнями белка. Они определили около 50 белков, которые присутствовали на более высоких или более низких уровнях в гипервозбудимых клетках Альцгеймера по сравнению со здоровыми клетками.
«Уже было известно, что некоторые из этих белков связаны с болезнью Альцгеймера, но многие — нет», — говорит Липтон.
Белки участвовали во многих разнообразных функциях нейронов, включая контроль над электронами свободных радикалов (редокс-модуляторы), энергетический обмен и воспаление. Пятнадцать белков оказались особенно высокими или низкими в нейронах, страдающих болезнью Альцгеймера, и группа Липтона планирует последующие исследования некоторых из этих молекул.
Он также планирует расширить использование scPatch-Clamp/Proteomics для скрининга наркотиков, проверяя, устраняют ли потенциальные лекарства от болезни Альцгеймера как гипервозбудимость нейронов, так и аномальные уровни белка. Он сопоставляет эти результаты с экспериментами на более крупных группах клеток мозга, полученных от пациентов с болезнью Альцгеймера, известных как церебральные органоиды или «мини-мозг».
«Одна клетка не всегда рассказывает всю историю», — объясняет Липтон. «Некоторые нарушения при болезни Альцгеймера связаны с тем, как клетки взаимодействуют друг с другом, поэтому, если мы сможем повторить такого рода исследование на органоиде мини-мозга, мы сможем сделать дополнительные открытия».
Липтон отмечает, что этот метод можно применить для разработки лекарств от других заболеваний, связанных с мозгом.
«Этот новый подход к персонализированной медицине, основанный на экспрессии белка и электрической активности одного нейрона, страдающего болезнью Альцгеймера, может совершить революцию в открытии лекарств не только для этого заболевания, но и для других неврологических заболеваний, которые значительно отстают от других терапевтических областей», — добавляет он.
Помимо Липтона и Йейтса, авторами исследования являются Свагата Гатак, Джолин К. Дидрих, Мария Талантова, Генри Скотт, Митал Шарма и Мэтью Альбертолл из Scripps Research; и Ниведита Бхадра и Николас Дж. Шорк из Научно-исследовательского института трансляционной геномики (профессор Шорк одновременно работает в Scripps Research).
Больше информации:
Swagata Ghatak et al., Одноклеточный патч-кламп/протеомика болезни Альцгеймера человека, возбуждающие нейроны, полученные из iPSC, в сравнении с изогенными контрольными клетками дикого типа, предполагает новую причинно-следственную связь и терапевтические цели, Передовая наука (2024). DOI: 10.1002/advs.202400545
Предоставлено Исследовательским институтом Скриппса
Цитирование: Ученые раскрывают новые молекулярные причины болезни Альцгеймера (2024 г., 22 мая), получено 23 мая 2024 г. с https://medicalxpress.com/news/2024-05-scientists-uncover-molecular-drivers-alzheimer.html.
Этот документ защищен авторским правом. За исключением любых добросовестных сделок в целях частного изучения или исследования, никакая часть не может быть воспроизведена без письменного разрешения. Содержимое предоставлено исключительно в информационных целях.